蛋白食品检验方法介绍
三聚氰胺[化学式C3H6N6]是一种重要的有机化工中间产品.它是一种纯白色单斜棱晶体,无味,熔点354℃;溶于热水,不溶于苯和四氯化碳,可溶于甲醇、甘油等.低毒,在一般情况下较稳定,但在高温下可能会分解放出氰化物.三聚氰胺没有任何营养价值.三聚氰胺是一种禁止用于宠物食品及动物饲料的化学物质,动物食用后可以使动物发生肾衰竭并导致死亡.
(1)根据上述信息我们知道三聚氰胺的化学性质有低毒,在一般情况下较稳定,但在高温下可能会分解放出氰化物.
(2)三聚氰胺中碳、氢、氮三种元素的质量比为6:1:14(或36:6:84),氮元素的质量分数为66.7%.
(3)某品牌牛奶的标签上标有:蛋白质含量2.8g(每100g),则喝一盒牛奶(180g)同时喝下蛋白质5.04g.
(4)蛋白质种类繁多.若牛奶中含有的蛋白质其平均含氮量为16%.则上述品牌牛奶中氮元素的含量为0.448(或0.45)g(每100g).
(5)检测食品中蛋白质含量的传统方法是:通过检测食品中氮元素的含量,推算其蛋白质含量.例如,若检测到牛奶中的氮元素质量分数≥0.46%,即为蛋白质含量检测合格.某种不合格牛奶中氮元素的质量分数为0.36%,若向1000g该牛奶中加入2g三聚氰胺,请计算此时牛奶中氮元素的质量分数,并根据计算结果说明不法分子在牛奶中添加三聚氰胺的目的.
解 析解:(1)由信息及化学性质是物质在化学反应中表现的性质,则低毒,在一般情况下较稳定,但在高温下可能会分解放出氰化物是该物质的化学性质,故答案为:低毒,在一般情况下较稳定,但在高温下可能会分解放出氰化物;
(2)由三聚氰胺的化学式为C3H6N6,则C、H、N元素的质量比为12×3:1×6:14×6=36:6:84=6:1:14,
氮元素的质量分数为 14×6
12×3+1×6+14×6×100%=66.7%,故答案为:6:1:14 (或36:6:84);66.7%;
(3)由100g牛奶中蛋白质含量2.8g,一盒牛奶的质量为180g,
则喝一盒牛奶同时喝下蛋白质为 180
100× 2.8=5.04g,故答案为:5.04;
(4)由100g牛奶中蛋白质含量2.8g,牛奶中含有的蛋白质其平均含氮量为16%,则氮元素的质量为2.8g×16%=0.448g≈0.45g,
故答案为:0.448(或0.45);
(5)由1000g该牛奶中加入2g三聚氰胺,则加入三聚氰胺后牛奶中氮元素的质量为1000g×0.36%+2g×66.7%≈4.9g,
此时牛奶中氮元素的质量分数为 4.9g
1000g+2g
×100%≈0.49%,
则牛奶中的氮元素质量分数≥0.46%,
目的是提高牛奶中含氮量,造成牛奶中蛋白质含量高或合格的假象等,
答:不法分子在牛奶中添加三聚氰胺的目的是提高氮元素的含量,造成牛奶中蛋白质含量高或合格的假象.
(1)根据信息中低毒,在一般情况下较稳定,但在高温下可能会分解放出氰化物来分析化学性质;
(2)根据物质的化学式,利用相对原子质量来计算元素的质量比及元素的质量分数;
(3)根据每100g牛奶中蛋白质含量2.8g,一盒牛奶的质量为180g来计算;
(4)根据蛋白质中的含氮元素的量及蛋白质的含量来计算;
(5)根据蛋白质和三聚氰胺中的氮元素质量来计算牛奶中的含氮量,进一步不法分子在牛奶中添加三聚氰胺的目的.
一、蛋白质食品检测方法基本原理(氮元素)
盐份(NaCl)是食品中最为常见的,像火腿、香肠、罐头食品、浓缩汤料和肉制品等。由于NaCL是易溶于水,所以常用的方法是溶解后的
样品,用硝酸银(AgNO3)做滴定剂,用终点滴定法滴定终点,滴定剂浓度至少为0.1mol/L。反应方程式为:
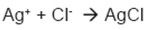
结果单位以%表示,即1g样品中含有多少mg的盐份(原子量=58.45g/mol)。
结果:
R = V(titr)* C(titr) * 58.45 * 10-3* 100%/m(smp)
R――――食品中盐份的含量,%
V(titr)――――到达终点时消耗的滴定剂(AgNO3)的体积,mL
C(titr)――――滴定剂(AgNO3)的浓度,mol/L
58.45――――氯化钠的分子量,g/mol
m(smp)――――样品重量,g
二、电极和试剂
MC6091Ag金属电极,复合银离子/参比电极(带CL114电缆)
AgNO3 标准溶液
0.1mol/L:取16.9873g分析纯级硝酸银溶解在100ml硝酸(1+1)中,用蒸馏水定容到1000mL(棕色容量瓶颈),硝酸银纯度很高,可以作为标准物质。
硝酸溶液:1mol/L。
三:实验步骤
1.开机,安装相应电极,进入管理员(supervisor)模式,在主窗口选择一个方法,在方法面板编辑方法,在电极面板编辑电极,在滴定剂面板编辑滴定剂、安装滴定剂以及输入浓度。(具体设置和操作见TIM
860 titration manager 操作说明书)。用蒸馏水清洗电极和滴定管。
2.一些主要的方法参数如下:
Burette volume: 25 ml
Stirring speed: 400 rpm
Working mode: mV (with i=0)
Number of end points: 1
End point: -100 mV
Stirring delay: 30 seconds
Minimum speed: 0.1 ml/min
Maximum speed: 4.0 ml/min
Proportional band: 200 mV
End point delay: 10 seconds
Sample unit: ml
Standard amount: 1g(取决于样品的量)
(depending on NaCl in the sample)
Titration: Increasing mV
Result1: ml
Result2: %
3.样品经过前处理后,准确量取处理好的样品于烧杯中,加入5ml的硝酸(1mol/L),如需要加入一定蒸馏水,放入搅拌子。把电极和滴定管插入样品中,注意不要让搅拌子碰到电极和滴定管。
4.运行方法。
5.保存结果。
如果要做几个平行样品,则清洗电极和滴定管,清洗小塑料瓶,然后加入新样品。
6.滴定操作完成后,为防止管路中的滴定剂被污染,把管路中的滴定剂排出,用蒸馏水清洗管路,然后用蒸馏水清洗滴定管和电极,MC6091Ag电极清洗后用电极帽套上;封好电极填充液口以防液体挥发,每次测量时检查填充液液面是否够高(不低于填充液口5毫米)。
7.直接从主机后面的开关关机。最后用防晒布把主机盖好。
(1)根据上述信息我们知道三聚氰胺的化学性质有低毒,在一般情况下较稳定,但在高温下可能会分解放出氰化物.
(2)三聚氰胺中碳、氢、氮三种元素的质量比为6:1:14(或36:6:84),氮元素的质量分数为66.7%.
(3)某品牌牛奶的标签上标有:蛋白质含量2.8g(每100g),则喝一盒牛奶(180g)同时喝下蛋白质5.04g.
(4)蛋白质种类繁多.若牛奶中含有的蛋白质其平均含氮量为16%.则上述品牌牛奶中氮元素的含量为0.448(或0.45)g(每100g).
(5)检测食品中蛋白质含量的传统方法是:通过检测食品中氮元素的含量,推算其蛋白质含量.例如,若检测到牛奶中的氮元素质量分数≥0.46%,即为蛋白质含量检测合格.某种不合格牛奶中氮元素的质量分数为0.36%,若向1000g该牛奶中加入2g三聚氰胺,请计算此时牛奶中氮元素的质量分数,并根据计算结果说明不法分子在牛奶中添加三聚氰胺的目的.
解 析解:(1)由信息及化学性质是物质在化学反应中表现的性质,则低毒,在一般情况下较稳定,但在高温下可能会分解放出氰化物是该物质的化学性质,故答案为:低毒,在一般情况下较稳定,但在高温下可能会分解放出氰化物;
(2)由三聚氰胺的化学式为C3H6N6,则C、H、N元素的质量比为12×3:1×6:14×6=36:6:84=6:1:14,
氮元素的质量分数为 14×6
12×3+1×6+14×6×100%=66.7%,故答案为:6:1:14 (或36:6:84);66.7%;
(3)由100g牛奶中蛋白质含量2.8g,一盒牛奶的质量为180g,
则喝一盒牛奶同时喝下蛋白质为 180
100× 2.8=5.04g,故答案为:5.04;
(4)由100g牛奶中蛋白质含量2.8g,牛奶中含有的蛋白质其平均含氮量为16%,则氮元素的质量为2.8g×16%=0.448g≈0.45g,
故答案为:0.448(或0.45);
(5)由1000g该牛奶中加入2g三聚氰胺,则加入三聚氰胺后牛奶中氮元素的质量为1000g×0.36%+2g×66.7%≈4.9g,
此时牛奶中氮元素的质量分数为 4.9g
1000g+2g
×100%≈0.49%,
则牛奶中的氮元素质量分数≥0.46%,
目的是提高牛奶中含氮量,造成牛奶中蛋白质含量高或合格的假象等,
答:不法分子在牛奶中添加三聚氰胺的目的是提高氮元素的含量,造成牛奶中蛋白质含量高或合格的假象.
(1)根据信息中低毒,在一般情况下较稳定,但在高温下可能会分解放出氰化物来分析化学性质;
(2)根据物质的化学式,利用相对原子质量来计算元素的质量比及元素的质量分数;
(3)根据每100g牛奶中蛋白质含量2.8g,一盒牛奶的质量为180g来计算;
(4)根据蛋白质中的含氮元素的量及蛋白质的含量来计算;
(5)根据蛋白质和三聚氰胺中的氮元素质量来计算牛奶中的含氮量,进一步不法分子在牛奶中添加三聚氰胺的目的.
一、蛋白质食品检测方法基本原理(氮元素)
盐份(NaCl)是食品中最为常见的,像火腿、香肠、罐头食品、浓缩汤料和肉制品等。由于NaCL是易溶于水,所以常用的方法是溶解后的
样品,用硝酸银(AgNO3)做滴定剂,用终点滴定法滴定终点,滴定剂浓度至少为0.1mol/L。反应方程式为:
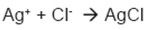
结果单位以%表示,即1g样品中含有多少mg的盐份(原子量=58.45g/mol)。
结果:
R = V(titr)* C(titr) * 58.45 * 10-3* 100%/m(smp)
R――――食品中盐份的含量,%
V(titr)――――到达终点时消耗的滴定剂(AgNO3)的体积,mL
C(titr)――――滴定剂(AgNO3)的浓度,mol/L
58.45――――氯化钠的分子量,g/mol
m(smp)――――样品重量,g
二、电极和试剂
MC6091Ag金属电极,复合银离子/参比电极(带CL114电缆)
AgNO3 标准溶液
0.1mol/L:取16.9873g分析纯级硝酸银溶解在100ml硝酸(1+1)中,用蒸馏水定容到1000mL(棕色容量瓶颈),硝酸银纯度很高,可以作为标准物质。
硝酸溶液:1mol/L。
三:实验步骤
1.开机,安装相应电极,进入管理员(supervisor)模式,在主窗口选择一个方法,在方法面板编辑方法,在电极面板编辑电极,在滴定剂面板编辑滴定剂、安装滴定剂以及输入浓度。(具体设置和操作见TIM
860 titration manager 操作说明书)。用蒸馏水清洗电极和滴定管。
2.一些主要的方法参数如下:
Burette volume: 25 ml
Stirring speed: 400 rpm
Working mode: mV (with i=0)
Number of end points: 1
End point: -100 mV
Stirring delay: 30 seconds
Minimum speed: 0.1 ml/min
Maximum speed: 4.0 ml/min
Proportional band: 200 mV
End point delay: 10 seconds
Sample unit: ml
Standard amount: 1g(取决于样品的量)
(depending on NaCl in the sample)
Titration: Increasing mV
Result1: ml
Result2: %
3.样品经过前处理后,准确量取处理好的样品于烧杯中,加入5ml的硝酸(1mol/L),如需要加入一定蒸馏水,放入搅拌子。把电极和滴定管插入样品中,注意不要让搅拌子碰到电极和滴定管。
4.运行方法。
5.保存结果。
如果要做几个平行样品,则清洗电极和滴定管,清洗小塑料瓶,然后加入新样品。
6.滴定操作完成后,为防止管路中的滴定剂被污染,把管路中的滴定剂排出,用蒸馏水清洗管路,然后用蒸馏水清洗滴定管和电极,MC6091Ag电极清洗后用电极帽套上;封好电极填充液口以防液体挥发,每次测量时检查填充液液面是否够高(不低于填充液口5毫米)。
7.直接从主机后面的开关关机。最后用防晒布把主机盖好。